第一部分:线上申请流程
临床研究管理委员会审查均在临床试验管理系统(以下简称:CTMS系统)进行线上立项申请,流程如下:
1. 院内申请:临床试验申请人在北京大学肿瘤医院内蒙古医院谷歌浏览器(内网) https://10.1.129.223 →CTMS系统申请注册系统账号,申请账号时按照系统提示要求上传临床试验申请人资质备案。创建院内工作人员帐号时,其用户名必须与临床试验申请人的HIS工号保持一致。
2. 院外申请:若属院外网络操作需向机构办递交《VPN开通审批表》(附件1.)(填法见附件2.)并签署《网络和信息安全承诺书-公司版》(附件3.)和《网络和信息安全承诺书-公司个人版》(附件4.),共三份文件,将扫描件打包发送至邮箱nmgzlyyGCP@126.com(邮件命名“VPN申请-公司-姓名”),随后致电机构办(0471-3281464)以确认。机构办OA申请流程。OA申请通过后,院外申请人能通过VPN链接(医院360零信任网关)访问CTMS系统并填写注册账号信息。(登录CTMS系统后,首页即可下载《医院360零信任网关使用手册》),VPN申请通过之日起的10个工作日内把附件1、3、4的签字盖章原件交至机构办完成备案。
3.注册CTMS账号说明:申办方在注册账号时要求CRA 备案上传附件,附件内容如下:《CRA人员信息登记表》(附件5)、《CRA 派遣函》(附件6;要求公司盖章)、CRA 简历(中文简历,需附照片,模板无要求)、身份证正反面复印件。
4. 机构办将在1个工作日内审核申请注册账号的信息,如注册信息有误驳回申请,申请人可再次注册,如注册信息符合要求审批通过,申请人可成功登陆系统。
5. 临床试验申请人登陆CTMS系统点击项目管理→新建(图一)→临床试验申请人填写临管会初始审查申请(图二)→主要研究者(PI)/科室主任/临管会秘书同步审核确认→临管会秘书分配临管会受理号→临管会委员函审→出具临管会意见/批件。
6. 临床试验申请人也可在CTMS系统→帮助中心→帮助文档,下载CTMS用户操作手册,根据手册说明进行操作。
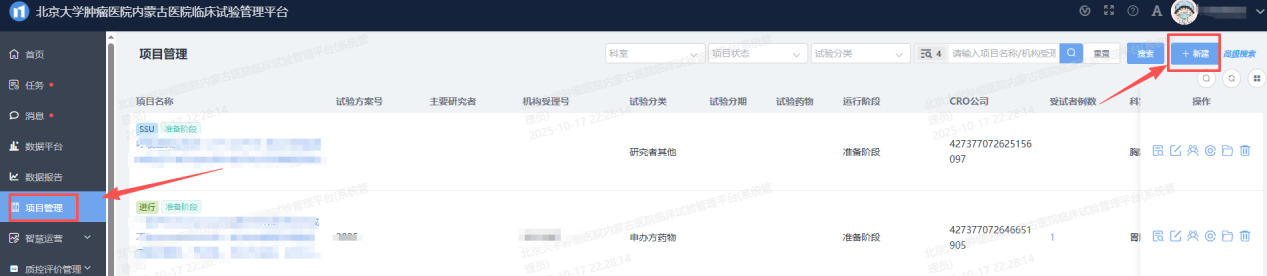
【申办方创建项目入口 图一】
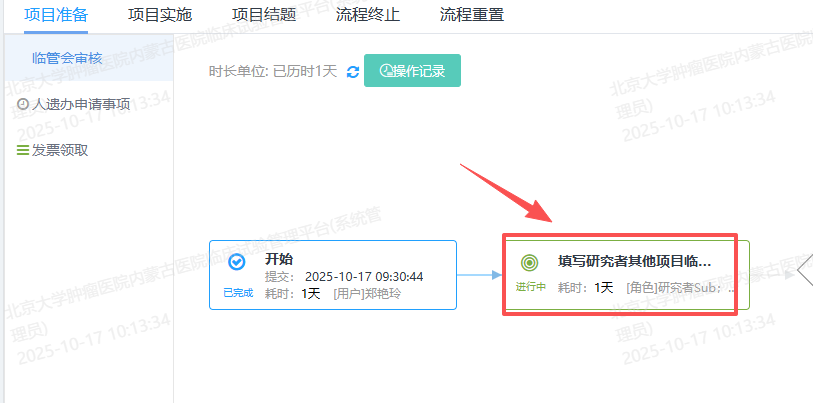
【临管会初始审查申请表入口 图二】
第二部分 线上立项须知
1. 临床试验申请人的立项申请首先须主要研究者(下称PI)在CTMS系统中审批同意立项后,方可流转至临管会秘书审核,请临床试验申请人及时获得PI批准。
2. 临管会秘书完成立项申请审核并分配受理号后,请申请人即刻上传电子版资料,并按《临床试验启动前立项SOP》(附件7或机构网页“北京大学肿瘤医院内蒙古医院药物临床试验立项审查流程”)所列清单,将纸质材料同步提交至临管会办公室(电话0471-3281464)。
3. 申办方发起项目初始审查申请单必须提供的材料清单:
(1) 主协议;
(2) 研究方案;
(3) 知情同意书;
(4) 项目负责人简历(提示:包括参与科研工作的情况介绍、GCP证书);
(5) 申办方资质;
(6) CDE批件(IND批件或IND受理单或IND通知书,均可);
(7) 经济利益声明表:如果在临管会初始审查申请表中的利益冲突的任意一个选项选择了“是”,则必须上传;
(8)主要sub-I授权书(附件8,如本研究有主要sub-I须提供此授权书,没有主要sub-I可不提供)。
4. 研究者发起项目初始审查申请单必须提供的材料清单:
(1) 主协议;
(2) 研究方案;
(3) 知情同意书;
(4) 项目负责人简历(提示:最新签字和日期的简历,包括参与科研工作的情况介绍、GCP证书);
(5) 国内未上市药物需提供:药物检测报告并加盖公司红章;
(6) 国内未上市但已在国内开展相关临床试验需提供:IND批件或IND通知书IND受理单;
(7) 国内未上市药物、凡涉及进口药物需提供:进口药物通关单;
(8) 超适应症研究需提供:药物使用说明书;
(9)主要sub-I授权书(附件8,如本研究有主要sub-I须提供此授权书,没有主要sub-I可不提供)。
以上材料经临管会形式审查通过后进行函审,截止每周三24:00前递交材料可本周五进行送审,逾期顺延至下周五进行送审。
网址:www.nmgzlyy.com 地址:呼和浩特市赛罕区昭乌达路42号
版权所有:北京大学肿瘤医院内蒙古医院•内蒙古医科大学附属肿瘤医院